Bereiche komplett auf- oder zuklappen:


2 Kompetenzbereiche, Inhaltsfelder und Kompetenzerwartungen
Die in den allgemeinen Aufgaben und Zielen des Faches beschriebene übergreifende fachliche Kompetenz wird ausdifferenziert, indem fachspezifische Kompetenzbereiche und Inhaltsfelder identifiziert und ausgewiesen werden. Dieses analytische Vorgehen erfolgt, um die Strukturierung der fachrelevanten Prozesse einerseits sowie der Gegenstände andererseits transparent zu machen. In den Kompetenzerwartungen werden beide Seiten miteinander verknüpft. Damit wird der Tatsache Rechnung getragen, dass der gleichzeitige Einsatz von Können und Wissen bei der Bewältigung von Anforderungssituationen eine zentrale Rolle spielt.
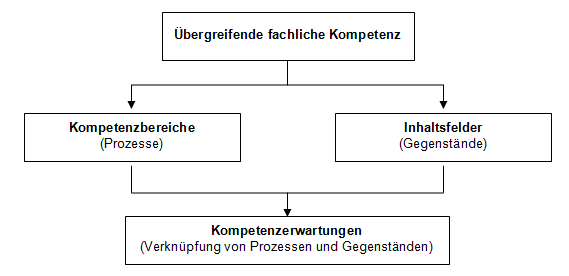
Kompetenzbereiche repräsentieren die Grunddimensionen des fachlichen Handelns. Sie dienen dazu, die einzelnen Teiloperationen entlang der fachlichen Kerne zu strukturieren und den Zugriff für die am Lehr-Lernprozess Beteiligten zu verdeutlichen.
Inhaltsfelder systematisieren mit ihren jeweiligen inhaltlichen Schwerpunkten die im Unterricht der Realschule verbindlichen und unverzichtbaren Gegenstände und liefern Hinweise für die inhaltliche Ausrichtung des Lehrens und Lernens.
Kompetenzerwartungen führen Prozesse und Gegenstände zusammen und beschreiben die fachlichen Anforderungen und intendierten Lernergebnisse, die in zwei Stufen bis zum Ende der Jahrgangstufe 10 verbindlich erreicht werden sollen. Kompetenzerwartungen
- beziehen sich auf beobachtbare Handlungen und sind auf die Bewältigung von Anforderungssituationen ausgerichtet,
- stellen im Sinne von Regelstandards die erwarteten Kenntnisse, Fähigkeiten und Fertigkeiten auf einem mittleren Abstraktionsgrad dar,
- ermöglichen die Darstellung einer Progression des Lernens bis zum Schulabschluss der Realschule und zielen auf kumulatives, systematisch vernetztes Lernen,
- können in Aufgabenstellungen umgesetzt und überprüft werden.
Insgesamt ist der Unterricht in der Realschule nicht allein auf das Erreichen der aufgeführten Kompetenzerwartungen beschränkt, sondern soll es Schülerinnen und Schülern ermöglichen, diese weiter auszubauen und darüber hinausgehende Kompetenzen zu erwerben.
2.1 Kompetenzbereiche und Inhaltsfelder des Faches
Der naturwissenschaftliche Unterricht in der Realschule ermöglicht den Erwerb von Kompetenzen, die insgesamt naturwissenschaftliche Grundbildung ausmachen. Das Fach Chemie leistet dazu wichtige Beiträge.
Kompetenzbereiche
In naturwissenschaftlichen Arbeitsprozessen werden meist Kompetenzen aus mehreren, nicht immer scharf voneinander abzugrenzenden Bereichen benötigt. Dieser Kernlehrplan unterscheidet die vier Kompetenzbereiche
- Umgang mit Fachwissen,
- Erkenntnisgewinnung,
- Kommunikation,
- Bewertung.
Der Kompetenzbereich Umgang mit Fachwissen bezieht sich auf die Fähigkeit von Schülerinnen und Schülern, zur Lösung von Aufgaben und Problemen fachbezogene Konzepte auszuwählen und zu nutzen. Ein Verständnis ihrer Bedeutung einschließlich der Abgrenzung zu ähnlichen Konzepten ist notwendig, um Wissen in variablen Situationen zuverlässig einsetzen zu können. Schülerinnen und Schüler können bei fachlichen Problemen besser auf ihr Wissen zugreifen, wenn sie dieses angemessen organisieren und strukturieren. Gut strukturierte Wissensbestände erleichtern ebenfalls die Integration und Vernetzung von neuem mit vorhandenem Wissen.
Der Kompetenzbereich Erkenntnisgewinnung beinhaltet die Fähigkeiten und methodischen Fertigkeiten von Schülerinnen und Schülern, naturwissenschaftliche Fragestellungen zu erkennen, diese mit Experimenten und anderen Methoden hypothesengeleitet zu untersuchen und Ergebnisse zu verallgemeinern. Naturwissenschaftliche Erkenntnis basiert im Wesentlichen auf einer Modellierung der Wirklichkeit. Modelle, von einfachen Analogien bis hin zu mathematisch-formalen Modellen, dienen dabei zur Veranschaulichung, Erklärung und Vorhersage. Eine Reflexion der Erkenntnismethoden verdeutlicht den besonderen Charakter der Naturwissenschaften mit seinen spezifischen Denk- und Arbeitsweisen und grenzt sie von anderen Möglichkeiten der Weltbegegnung ab.
Der Kompetenzbereich Kommunikation beschreibt erforderliche Fähigkeiten für einen produktiven fachlichen Austausch. Kennzeichnend dafür ist, mit Daten und Informationsquellen sachgerecht und kritisch umzugehen sowie fachsprachliche Ausführungen in schriftlicher und mündlicher Form verstehen und selbst präsentieren zu können. Dazu gehört auch, gebräuchliche Darstellungsformen wie Tabellen, Graphiken, Diagramme zu beherrschen sowie bewährte Regeln der fachlichen Argumentation einzuhalten. Charakteristisch für die Naturwissenschaften sind außerdem das Offenlegen eigener Überlegungen bzw. die Akzeptanz fremder Ideen und das Arbeiten in Gemeinschaften und Teams.
Der Kompetenzbereich Bewertung bezieht sich auf die Fähigkeit, überlegt zu urteilen. Dazu gehört, Kriterien und Handlungsmöglichkeiten sorgfältig zusammenzutragen und gegeneinander abzuwägen. Auf dieser Grundlage ist es möglich, Entscheidungen zu finden und dafür zielführend zu argumentieren und Position zu beziehen. Für gesellschaftliche und persönliche Entscheidungen sind diesbezüglich die Kenntnis und Berücksichtigung von normativen und ethischen Maßstäben bedeutsam, nach denen Interessen und Folgen naturwissenschaftlicher Forschung beurteilt werden können.
Inhaltsfelder im Fach Chemie
Kompetenzen sind stets an fachliche Inhalte gebunden und basieren auf einem gut abrufbaren strukturierten Fachwissen. Dieses wird in den folgenden Inhaltsfeldern erworben, die hinreichend Gelegenheiten bieten, chemische Fragestellungen, Sachverhalte, Konzepte und Arbeitsweisen zu erschließen. Das Fachwissen wird über die verschiedenen Inhaltsfelder hinweg durch die Basiskonzepte strukturiert und vernetzt.
Die Nummerierung der Inhaltsfelder dient der Orientierung in den nachfolgenden Kapiteln des Lehrplans. Bei der Überführung der Inhaltsfelder und der zugeordneten inhaltlichen Schwerpunkte in konkrete Unterrichtsvorhaben können nach Entscheidung der Fachkonferenz von den Vorgaben abweichende Zuordnungen entstehen, sofern diese innerhalb der vorgegebenen Progressionsstufen erfolgen.
Stoffe und Stoffeigenschaften (1)
Schülerinnen und Schüler werden täglich mit einer Vielzahl von Stoffen konfrontiert, deren Zusammensetzung bzw. Nutzen oder Funktion sich ihnen nicht unmittelbar erschließt. Wissen über Einsatzbereiche, Anwendungen und mögliche Gefahren verschiedener Stoffe ist jedoch notwendig, um sinnvolle Entscheidungen zu ihrer Verwendung treffen zu können. Hilfreich sind hier erste Klassifizierungsmerkmale sowie Verfahren, Stoffe anhand ihrer Eigenschaften voneinander zu unterscheiden. Wesentlich sind dabei auch Änderungen ihres Zustands. Der materielle Aufbau von Stoffen und Änderungen ihrer Aggregatzustände lassen sich mit einfachen Teilchenmodellen beschreiben und erklären. Von besonderer Bedeutung für die Chemie sind Stofftrennungen.
Energieumsätze bei Stoffveränderungen (2)
Chemische Reaktionen beschreiben Vorgänge, bei denen eine oder mehrere chemische Verbindungen unter Beteiligung von Energie in andere umgewandelt werden. Dabei können sich die Eigenschaften der Produkte im Vergleich zu den Ausgangsstoffen stark ändern. Die Oxidation bei Verbrennungen ist dafür ein Beispiel. Ob Lagerfeuer oder Zentralheizung, ob gewollte Verbrennung oder Brandkatastrophe, das Wissen um die chemischen Grundlagen solcher Prozesse dient auch als Ausgangspunkt für angemessenes Handeln. Wirksame Maßnahmen zur Brandverhinderung und Brandbekämpfung fördern die eigene Sicherheit und gelten als gesellschaftlich notwendige Aufgaben. Auch für einen reflektierten Umgang mit Energieressourcen sind Kenntnisse über die bei Verbrennungen anfallenden Produkte und über die ablaufenden Vorgänge wichtige Voraussetzungen.
Luft und Wasser (3)
Luft und Wasser gehören zu den lebensnotwendigen Ressourcen. Sie sind für alle Lebewesen, aber auch für viele technische Abläufe unverzichtbar. Ähnlich wichtig sind die Bestandteile der Luft. Die in ihr enthaltenen Gase bestimmen den Aufbau der Atmosphäre und ermöglichen die Existenz von Leben auf der Erde. Der Mensch nimmt in vielfältiger Art und Weise Einfluss auf die Qualität dieser Ressourcen. Dabei ist es notwendig, ein entsprechendes Bewusstsein für den Schutz und eine nachhaltige Nutzung von Wasser und Luft zu entwickeln.
Metalle und Metallgewinnung (4)
Die Geschichte der Menschheit ist eng mit der Nutzung von Metallen verbunden. Metalle und ihre Legierungen zeichnen sich durch Eigenschaften aus, die bei der Herstellung und Verwendung von Gebrauchsgegenständen und Arbeitsgeräten besonders vorteilhaft sind. Metalle kommen meist in der Natur nicht elementar vor, sondern müssen aus Erzen gewonnen werden. Dies geschieht über chemische Prozesse, in denen mithilfe von Redoxreaktionen Umwandlungen von Metallverbindungen vorgenommen werden. Das Verständnis gebräuchlicher Verfahren der Metallgewinnung ermöglicht die Einsicht in einen verantwortungsvollen Umgang mit Rohstoff- und Energieressourcen und zeigt die Notwendigkeit des Recyclings auf.
Elemente und ihre Ordnung (5)
Ziel der Chemie ist es, Veränderungen von Stoffen nicht nur klassifizieren und beschreiben zu können, sondern diese Veränderungen über Modelle des Aufbaus der Materie zu erklären. Eine Systematik des Aufbaus der Materie wird in einem einfachen und universellen Ordnungssystem durch das Periodensystem der Elemente dargestellt. Es beschreibt Beziehungen und Verwandtschaften der Elemente und dient auch als Quelle für Informationen zum Atombau.
Säuren, Basen, Salze (6)
Säuren, Laugen und Salzesind in vielen verschiedenen Kontexten des Alltags und der Lebenswelt anzutreffen. Sie sind u. a. Bestandteil von Reinigungsmitteln, Konservierungsstoffen und Düngemitteln. Eigenschaften und der Aufbau von Salzen aus Ionen, der Zusammenhalt im Ionengitter sowie die Neutralisation als Reaktion von Säuren und Laugen lassen sich mit einfachen Modellen anschaulich erklären. Eine besondere Rolle spielt hier das Wasser als Lösungsmittel. Vielen sauren und alkalischen Lösungen und Salzen begegnet man auch in der Berufs- und Arbeitswelt, vor allem in den Bereichen Landwirtschaft und Ernährung. Hier sind Kenntnisse über die Wirkung, den Einsatz und die sichere Handhabung dieser Stoffe aus gesundheitlichen Gründen erforderlich.
Energie aus chemischen Reaktionen (7)
Die Umwandlung von chemischer in elektrische Energie bildet die Grundlage für die Funktion mobiler Energiespeicher. In ihnen laufen Elektronenübertragungsreaktionen ab. Teilweise lassen sich die chemischen Reaktionen durch erzwungene Elektronenübertragungen bei Ladevorgängen wieder umkehren. Für moderne Kommunikations- und Unterhaltungsgeräte sowie Fahrzeuge werden zunehmend Batterien bzw. Akkumulatoren als Energiequellen eingesetzt. Mit Blick auf eine nachhaltige Energienutzung werden Anstrengungen zur Entwicklung neuer Energiespeicher und Brennstoffzellen unternommen. Erzwungene Elektronenübertragungen werden auch für die Veredlung von Metalloberflächen genutzt.
Stoffe als Energieträger (8)
Als Primär- oder Rohenergieträger bezeichnet man Energieträger, die in der Natur zur Verfügung stehen. Die meisten dieser Stoffe sind organischen Ursprungs. Ihre Struktur-Eigenschafts-Beziehungen bestimmen die molekulare Vielfalt organischer Verbindungen. Natürliche Energieträger wie Erdöl werden industriell aufbereitet, um Nutzenergie (Wärme, Bewegung, Licht) bei Bedarf zur Verfügung zu stellen. Die Weiterverarbeitung dieser organischen Stoffe in wichtigen Zweigen der chemischen Industrie eröffnet zahlreiche Arbeits- und Berufsfelder. Es ergibt sich die Notwendigkeit, durch Verwendung nachwachsender Rohstoffe und durch Recycling schonend mit den knappen natürlichen Ressourcen umzugehen.
Produkte der Chemie (9)
In Deutschland ist die Chemieproduktion ein wichtiger Industriezweig. Zur Vielfalt der erzeugten Produkte gehören Artikel des täglichen Bedarfs wie Seifen und Waschmittel, Kosmetika und Körperpflegemittel, Duft- und Aromastoffe, aber auch Lebensmittel sowie neue Bau- und Werkstoffe. Der Aufbau sowie einfache Strukturen und Funktionen dieser Stoffe unterliegen gemeinsamen Prinzipien. Durch aktuelle chemische Forschung werden gezielt neue Produkte für spezielle Verwendungen entwickelt. Dabei ergeben sich einerseits neue Chancen zur Verbesserung unserer Lebensbedingungen, andererseits können aber auch Risiken in der Anwendung und im Produktionsprozess entstehen, die bewertet und beherrscht werden müssen.
2.2 Kompetenzerwartungen und zentrale Inhalte der ersten Progressionsstufe
Der Unterricht soll es den Schülerinnen und Schülern ermöglichen, am Ende einer ersten Progressionsstufe, die in der Regel nach etwa einem Drittel der bis Ende des Jg. 10 vorgesehenen Unterrichtszeit erreicht wird, über die im Folgenden genannten Kompetenzen zu verfügen. Dabei werden zunächst die Kompetenzbereiche in Form übergeordneter Kompetenzen ausdifferenziert, wobei auch deren Weiterentwicklung in der zweiten Progressionsstufe (s. Kap. 2.3) gesehen werden muss. Die übergeordneten Kompetenzen werden im Anschluss daran mit den verpflichtenden Inhalten zu Kompetenzerwartungen zusammengeführt und somit inhaltsfeldbezogen konkretisiert.
Kompetenzbereich Umgang mit Fachwissen
Schülerinnen und Schüler können …
|
UF1 Fakten wiedergeben und erläutern |
Phänomene und Vorgänge mit einfachen chemischen Konzepten beschreiben und erläutern. |
|
UF2 Konzepte unterscheiden und auswählen |
bei der Beschreibung chemischer Sachverhalte Fachbegriffe angemessen und korrekt verwenden. |
|
UF3 Sachverhalte ordnen und strukturieren |
chemische Objekte und Vorgänge nach vorgegebenen Kriterien ordnen. |
|
UF4 Wissen vernetzen |
Alltagsvorstellungen kritisch infrage stellen und gegebenenfalls durch chemische Konzepte ergänzen oder ersetzen. |
Kompetenzbereich Erkenntnisgewinnung
Schülerinnen und Schüler können …
|
E1 Fragestellungen erkennen |
chemische Fragestellungen von anderen Fragestellungen unterscheiden. |
|
E2 Bewusst wahrnehmen |
Phänomene nach vorgegebenen Kriterien beobachten und zwischen der Beschreibung und der Deutung einer Beobachtung unterscheiden. |
|
E3 Hypothesen entwickeln |
Vermutungen zu chemischen Fragestellungen mit Hilfe von Alltagswissen und einfachen fachlichen Konzepten begründen. |
|
E4 Untersuchungen und Experimente planen |
vorgegebene Versuche begründen und einfache Versuche selbst entwickeln. |
|
E5 Untersuchungen und Experimente durchführen |
Untersuchungsmaterialien nach Vorgaben zusammenstellen und unter Beachtung von Sicherheits- und Umweltaspekten nutzen. |
|
E6 Untersuchungen und Experimente auswerten |
Beobachtungen und Messdaten mit Bezug auf eine Fragestellung schriftlich festhalten, daraus Schlussfolgerungen ableiten und Ergebnisse verallgemeinern. |
|
E7 Modelle auswählen und Modellgrenzen angeben |
einfache Modelle zur Veranschaulichung chemischer Zusammenhänge beschreiben und Abweichungen der Modelle von der Realität angeben. |
|
E8 Modelle anwenden |
chemische Phänomene mit einfachen Modellvorstellungen erklären. |
|
E9 Arbeits- und Denkweisen reflektieren |
in einfachen chemischen Zusammenhängen Aussagen auf Stimmigkeit überprüfen. |
Kompetenzbereich Kommunikation
Schülerinnen und Schüler können …
|
K1 Texte lesen und erstellen |
altersgemäße Texte mit chemischen Inhalten Sinn entnehmend lesen und sinnvoll zusammenfassen. |
|
K2 Informationen identifizieren |
relevante Inhalte fachtypischer bildlicher Darstellungen wiedergeben sowie Werte aus Tabellen und einfachen Diagrammen ablesen. |
|
K3 Untersuchungen dokumentieren |
bei Untersuchungen und Experimenten Fragestellungen, Handlungen, Beobachtungen und Ergebnisse nachvollziehbar schriftlich festhalten. |
|
K4 Daten aufzeichnen und darstellen |
Beobachtungs- und Messdaten in Tabellen übersichtlich aufzeichnen und in vorgegebenen einfachen Diagrammen darstellen. |
|
K5 Recherchieren |
Informationen zu vorgegebenen chemischen Begriffen in ausgewählten Quellen finden und zusammenfassen. |
|
K6 Informationen umsetzen |
auf der Grundlage vorgegebener Informationen Handlungsmöglichkeiten benennen. |
|
K7 Beschreiben, präsentieren, begründen |
chemische Sachverhalte, Handlungen und Handlungsergebnisse für andere nachvollziehbar beschreiben und begründen. |
|
K8 Zuhören, hinterfragen |
bei der Klärung chemischer Fragestellungen anderen konzentriert zuhören, deren Beiträge zusammenfassen und bei Unklarheiten sachbezogen nachfragen. |
|
K9 Kooperieren und im Team arbeiten |
mit einem Partner oder in einer Gruppe gleichberechtigt, zielgerichtet und zuverlässig arbeiten und dabei unterschiedliche Sichtweisen achten. |
Kompetenzbereich Bewertung
Schülerinnen und Schüler können …
|
B1 Bewertungen an Kriterien orientieren |
in einfachen Zusammenhängen eigene Bewertungen und Entscheidungen unter Verwendung chemischen Wissens begründen. |
|
B2 Argumentieren und Position beziehen |
bei gegensätzlichen Ansichten Sachverhalte nach vorgegebenen Kriterien und vorliegenden Fakten beurteilen. |
|
B3 Werte und Normen berücksichtigen |
Wertvorstellungen, Regeln und Vorschriften in chemisch-technischen Zusammenhängen hinterfragen und begründen. |
Im Folgenden werden die Inhaltsfelder, in denen sich Kompetenzen der Schülerinnen und Schüler entwickeln, näher beschrieben. Zur Eingrenzung und Konkretisierung der Inhaltsfelder sind verbindliche inhaltliche Schwerpunkte angegeben. Ebenfalls angegeben sind mögliche Kontexte, in denen die Inhalte erarbeitet werden können. Diese Vorschläge können durch sinnvolle andere Kontexte ersetzt werden, wenn sie in gleicher Weise problemorientiertes und aktives Lernen sowie den Erwerb der geforderten Kompetenzen ermöglichen.
Die Beschreibung der Inhaltsfelder wird ergänzt durch Angaben zu anschlussfähigen fachlichen Konzepten, über die Schülerinnen und Schüler im Rahmen der verbindlichen Kompetenzerwartungen verfügen sollen. Die Strukturierung durch Basiskonzepte entspricht dabei deren doppelter Funktion, Inhalte situationsübergreifend zu vernetzen und Perspektiven für Fragestellungen zu eröffnen. Die genannten fachlichen Konzepte besitzen nicht nur Bedeutung im jeweiligen Inhaltsfeld, sondern sollten in unterschiedlichen Zusammenhängen immer wieder aufgegriffen und vertieft werden.
Bezieht man die übergeordneten Kompetenzerwartungen sowie die Inhaltsfelder aufeinander, so ergeben sich die nachfolgenden konkretisierten Kompetenzerwartungen. Sie beschreiben verbindliche Erwartungen an die Kompetenzen von Schülerinnen und Schülern am Ende einer ersten Progressionsstufe der Kompetenzentwicklung. Sie schreiben jedoch keinen besonderen Unterrichtsgang zum Erwerb dieser Kompetenzen vor. Es wird erwartet, dass Schülerinnen und Schüler nicht nur im beschriebenen Zusammenhang, sondern auch in anderen Situationen zeigen, dass sie die geforderten Kompetenzen besitzen.
Hinter den inhaltsbezogenen Kompetenzbeschreibungen ist jeweils in Klammern angegeben, welche übergeordneten Kompetenzerwartungen durch diese konkretisiert werden. Mehrfachnennungen verdeutlichen, dass in der Praxis oft mehrere Komponenten kompetenten Handelns wirksam werden, wobei Schwerpunkte an erster Stelle genannt werden.
Inhaltsfeld Stoffe und Stoffeigenschaften (1)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
|
|
Basiskonzept Chemische Reaktion Dauerhafte Eigenschaftsänderungen von Stoffen Basiskonzept Struktur der Materie Aggregatzustände, Teilchenvorstellungen, Lösungsvorgänge, Kristalle Basiskonzept Energie Wärme, Schmelz- und Siedetemperatur, Aggregatzustandsänderungen |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- Ordnungsprinzipien für Stoffe nennen und diese in Stoffgemische und Reinstoffe einteilen. (UF3)
- charakteristische Stoffeigenschaften zur Unterscheidung bzw. Identifizierung von Stoffen beschreiben und die Verwendung von Stoffen ihren Eigenschaften zuordnen. (UF2, UF3
- einfache Trennverfahren für Stoffe und Stoffgemische beschreiben. (UF1)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- einfache Versuche (u. a. zur Trennung von Stoffen in Stoffgemischen unter Nutzung relevanter Stoffeigenschaften) planen und sachgerecht durchführen. (E4, E5)
- Messreihen zu Temperaturänderungen durchführen und zur Aufzeichnung der Messdaten einen angemessenen Temperaturbereich und sinnvolle Zeitintervalle wählen. (E5, E6)
- Stoffe, Stofftrennungen, Aggregatzustände und Übergänge zwischen ihnen mit Hilfe eines Teilchenmodells erklären. (E7, E8)
Kommunikation
Die Schülerinnen und Schüler können …
- Texte mit chemierelevanten Inhalten in Schulbüchern und in altersgemäßen populärwissenschaftlichen Schriften Sinn entnehmend lesen und zusammenfassen. (K1, K2)
- fachtypische, einfache Zeichnungen von Versuchsaufbauten erstellen. (K7)
- einfache Darstellungen oder Modelle verwenden, um Aggregatzustände und Lösungsvorgänge zu veranschaulichen und zu erläutern. (K7)
- bei Versuchen in Kleingruppen (u. a. zu Stofftrennungen) Initiative und Verantwortung übernehmen, Aufgaben fair verteilen und diese im verabredeten Zeitrahmen sorgfältig erfüllen. (K9, K8)
- Messdaten in ein vorgegebenes Koordinatensystem eintragen und gegebenenfalls durch eine Messkurve verbinden sowie aus Diagrammen Messwerte ablesen. (K4, K2)
- Schmelz- und Siedekurven interpretieren und Schmelz- und Siedetemperaturen aus ihnen ablesen. (K2)
Bewertung
Die Schülerinnen und Schüler können …
- geeignete Maßnahmen zum sicheren und umweltbewusstem Umgang mit Stoffen nennen und umsetzen. (B3)
- Trennverfahren nach ihrer Angemessenheit beurteilen. (B1)
Inhaltsfeld Stoff- und Energieumsätze bei chemischen
Reaktionen (2)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
|
|
|
|
Basiskonzept Chemische Reaktion Gesetz von der Erhaltung der Masse, Umgruppierung von Teilchen Basiskonzept Struktur der Materie Element, Verbindung, einfaches Teilchenmodell Basiskonzept Energie Chemische Energie, Aktivierungsenergie, exotherme und endotherme Reaktion |
||
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- Reinstoffe aufgrund ihrer Zusammensetzung in Elemente und Verbindungen einteilen und Beispiele dafür nennen. (UF3)
- die Bedingungen für einen Verbrennungsvorgang beschreiben und auf dieser Basis Brandschutzmaßnahmen erläutern. (UF1)
- chemische Reaktionen, bei denen Sauerstoff aufgenommen wird, als Oxidation einordnen. (UF3)
- die Bedeutung der Aktivierungsenergie zum Auslösen einer chemischen Reaktion erläutern. (UF1)
- ein einfaches Atommodell (Dalton) beschreiben und zur Veranschaulichung nutzen. (UF1)
- Stoffumwandlungen als chemische Reaktionen von physikalischen Veränderungen abgrenzen. (UF2, UF3)
- an Beispielen die Bedeutung des Gesetzes von der Erhaltung der Masse durch die konstante Atomanzahl erklären. (UF1)
Erkenntnisgewinnung
Schülerinnen und Schüler können …
- Glut- oder Flammenerscheinungen nach vorgegebenen Kriterien beobachten und beschreiben, als Oxidationsreaktionen interpretieren und mögliche Edukte und Produkte benennen. (E2, E6)
- konkrete Vorschläge über verschiedene Möglichkeiten der Brandlöschung machen und diese mit dem Branddreieck begründen. (E3)
- Sauerstoff und Kohlenstoffdioxid experimentell nachweisen und die Nachweisreaktion beschreiben. (E4, E5)
- für die Oxidation bekannter Stoffe ein Reaktionsschema in Worten formulieren. (E8)
- bei Oxidationsreaktionen Massenänderungen von Reaktionspartnern vorhersagen und mit der Umgruppierung von Atomen erklären. (E3, E8)
- Grundgedanken der Phlogistontheorie als überholte Erklärungsmöglichkeit für das Phänomen Feuer erläutern und mit heutigen Vorstellungen vergleichen. (E9)
Kommunikation
Die Schülerinnen und Schüler können …
- Verfahren des Feuerlöschens in Modellversuchen demonstrieren. (K7)
- aufgrund eines Energiediagramms eine chemische Reaktion begründet als exotherme oder endotherme Reaktion einordnen. (K2)
- Gefahrstoffsymbole und Gefahrstoffhinweise erläutern und Verhaltensweisen im Umgang mit entsprechenden Stoffen beschreiben. (K6)
Bewertung
Die Schülerinnen und Schüler können …
- die Brennbarkeit von Stoffen bewerten und Sicherheitsregeln im Umgang mit brennbaren Stoffen und offenem Feuer begründen. (B1, B3)
- fossile und regenerative Brennstoffe unterscheiden und deren Nutzung unter den Aspekten Ökologie und Nachhaltigkeit beurteilen. (B2)
Inhaltsfeld Luft und Wasser (3)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
|
|
Basiskonzept Chemische Reaktion Nachweis von Wasser, Sauerstoff und Wasserstoff, Analyse und Synthese von Wasser Basiskonzept Struktur der Materie Luftzusammensetzung, Anomalie des Wassers Basiskonzept Energie Wärme, Wasserkreislauf |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- die wichtigsten Bestandteile und die prozentuale Zusammensetzung des Gasgemisches Luft benennen. (UF1)
- Ursachen und Vorgänge der Entstehung von Luftschadstoffen und deren Wirkungen erläutern. (UF1)
- Treibhausgase benennen und den Treibhauseffekt mit der Wechselwirkung von Strahlung mit der Atmosphäre erklären. (UF1)
- Wasser als Verbindung von Wasserstoff und Sauerstoff beschreiben und die Synthese und Analyse von Wasser als umkehrbare Reaktionen darstellen. (UF2)
- die besondere Bedeutung von Wasser mit dessen Eigenschaften (Anomalie des Wassers, Lösungsverhalten) erklären. (UF3)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- Wasser und die bei der Zersetzung von Wasser entstehenden Gase experimentell nachweisen und die Nachweisreaktionen beschreiben. (E4, E5)
- ein Verfahren zur Bestimmung des Sauerstoffgehalts der Luft erläutern. (E4, E5)
- Kriterien zur Bestimmung der Wasser- und Gewässergüte angeben. (E4)
Kommunikation
Die Schülerinnen und Schüler können …
- typische Merkmale eines naturwissenschaftlich argumentierenden Sachtexts aufzeigen. (K1)
- aus Tabellen oder Diagrammen Gehaltsangaben (in g/l oder g/cm³ bzw. in Prozent) entnehmen und interpretieren. (K2)
- Messwerte (u. a. zu Belastungen der Luft und des Wassers mit Schadstoffen) aus Tabellen herauslesen und in Diagrammen darstellen. (K2, K4)
- zuverlässigen Quellen im Internet aktuelle Messungen zu Umweltdaten entnehmen. (K2, K5)
- Beiträgen anderer bei Diskussionen über chemische Ideen und Sachverhalte konzentriert zuhören und bei eigenen Beiträgen sachlich Bezug auf deren Aussagen nehmen. (K8)
Bewertung
Die Schülerinnen und Schüler können …
- Gefährdungen von Luft und Wasser durch Schadstoffe anhand von Grenzwerten beurteilen und daraus begründet Handlungsbedarf ableiten. (B2, B3)
- die gesellschaftliche Bedeutung des Umgangs mit Trinkwasser auf lokaler Ebene und weltweit vor dem Hintergrund der Nachhaltigkeit bewerten. (B3)
Inhaltsfeld Metalle und Metallgewinnung (4)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
|
|
Basiskonzept Chemische Reaktion Oxidation, Reduktion, Redoxreaktion Basiskonzept Struktur der Materie Edle und unedle Metalle, Legierungen Basiskonzept Energie Energiebilanzen, endotherme und exotherme Redoxreaktionen |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- wichtige Gebrauchsmetalle und Legierungen benennen, deren typische Eigenschaften beschreiben und Metalle von Nichtmetallen unterscheiden. (UF1)
- den Weg der Metallgewinnung vom Erz zum Roheisen und Stahl beschreiben. (UF1)
- chemische Reaktionen, bei denen Sauerstoff abgegeben wird, als Reduktion einordnen. (UF3)
- chemische Reaktionen, bei denen es zu einer Sauerstoffübertragung kommt, als Redoxreaktion einordnen. (UF3)
- Korrosion als Oxidation von Metallen erklären und einfache Maßnahmen zum Korrosionsschutz erläutern. (UF4)
- an einfachen Beispielen die Gesetzmäßigkeit der konstanten Atomanzahlverhältnisse erläutern. (UF1)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- auf der Basis von Versuchsergebnissen unedle und edle Metalle anordnen und diese Anordnung zur Vorhersage von Redoxreaktionen nutzen. (E6, E3)
- Versuche zur Reduktion von ausgewählten Metalloxiden selbstständig planen und dafür sinnvolle Reduktionsmittel benennen. (E4)
- für eine Redoxreaktion ein Reaktionsschema als Wortgleichung und als Reaktionsgleichung formulieren und dabei die Oxidations- und Reduktionsvorgänge kennzeichnen. (E8)
- zur Klärung chemischer Fragstellungen (u. a. zu den Ursachen des Rostens) unterschiedliche Versuchsbedingungen schaffen und systematisch verändern. (E5)
- darstellen, warum Metalle Zeitaltern ihren Namen gegeben, den technischen Fortschritt beeinflusst sowie neue Berufe geschaffen haben. (E9)
Kommunikation
Die Schülerinnen und Schüler können …
- Experimente in einer Weise protokollieren, die eine nachträgliche Reproduktion der Ergebnisse ermöglicht. (K3)
- Möglichkeiten der Nutzung und Gewinnung von Metallen und ihren Legierungen in verschiedenen Quellen recherchieren und Abläufe folgerichtig unter Verwendung relevanter Fachbegriffe darstellen. (K5, K1, K7)
- in einem kurzen, zusammenhängenden Vortrag chemische Zusammenhänge (z. B. im Bereich Metallgewinnung) anschaulich darstellen. (K7)
Bewertung
Die Schülerinnen und Schüler können …
- die Bedeutung des Metallrecyclings im Zusammenhang mit Ressourcenschonung und Energieeinsparung darstellen und auf dieser Basis das eigene Konsum- und Entsorgungsverhalten beurteilen. (B3)
2.3 Kompetenzerwartungen und zentrale Inhalte der zweiten Progressionsstufe
Der Unterricht der zweiten Progressionsstufe baut auf der Kompetenzentwicklung der ersten Stufe auf, nutzt die dort erworbenen Kompetenzen und erweitert sie entsprechend. Bis zum Ende der Jahrgangsstufe 10 sollen die Schülerinnen und Schüler über die im Folgenden genannten Kompetenzen verfügen. Dabei werden zunächst übergeordnete Kompetenzen zu allen Kompetenzbereichen aufgeführt. Diese werden im Anschluss an die Erläuterung des Inhaltsfelds zusätzlich inhaltsfeldbezogen konkretisiert.
Kompetenzbereich Umgang mit Fachwissen
Schülerinnen und Schüler können …
|
UF1 Fakten wiedergeben und erläutern |
Konzepte der Chemie an Beispielen erläutern und dabei Bezüge zu Basiskonzepten und übergeordneten Prinzipien herstellen. |
|
UF2 Konzepte unterscheiden und auswählen |
chemische Konzepte und Analogien für Problemlösungen begründet auswählen und dabei zwischen wesentlichen und unwesentlichen Aspekten unterscheiden. |
|
UF3 Sachverhalte ordnen und strukturieren |
Prinzipien zur Strukturierung und zur Verallgemeinerung chemischer Sachverhalte entwickeln und anwenden. |
|
UF4 Wissen vernetzen |
vielfältige Verbindungen zwischen Erfahrungen und Konzepten innerhalb und außerhalb der Chemie herstellen und anwenden. |
Kompetenzbereich Erkenntnisgewinnung
Schülerinnen und Schüler können …
|
E1 Fragestellungen erkennen |
chemische Probleme erkennen, in Teilprobleme zerlegen und dazu Fragestellungen formulieren. |
|
E2 Bewusst wahrnehmen |
Kriterien für Beobachtungen entwickeln und die Beschreibung einer Beobachtung von ihrer Deutung klar abgrenzen. |
|
E3 Hypothesen entwickeln |
zu chemischen Fragestellungen begründete Hypothesen formulieren und Möglichkeiten zu ihrer Überprüfung angeben. |
|
E4 Untersuchungen und Experimente planen |
zu untersuchende Variablen identifizieren und diese in Experimenten systematisch verändern bzw. konstant halten. |
|
E5 Untersuchungen und Experimente durchführen |
Untersuchungen und Experimente selbstständig, zielorientiert und sachgerecht durchführen und dabei mögliche Fehlerquellen benennen. |
|
E6 Untersuchungen und Experimente auswerten |
Aufzeichnungen von Beobachtungen und Messdaten bezüglich einer Fragestellung interpretieren, daraus qualitative und einfache quantitative Zusammenhänge ableiten und diese formal beschreiben. |
|
E7 Modelle auswählen und Modellgrenzen angeben |
Modelle zur Erklärung von Phänomenen begründet auswählen und dabei ihre Grenzen und Gültigkeitsbereiche. angeben. |
|
E8 Modelle anwenden |
Modelle, auch in formalisierter oder mathematischer Form, zur Beschreibung, Erklärung und Vorhersage verwenden. |
|
E9 Arbeits- und Denkweisen reflektieren |
anhand historischer Beispiele die Vorläufigkeit chemischer Regeln, Gesetze und theoretischer Modelle beschreiben. |
Kompetenzbereich Kommunikation
Schülerinnen und Schüler können …
|
K1 Texte lesen und erstellen |
chemische Zusammenhänge sachlich und sachlogisch strukturiert schriftlich darstellen. |
|
K2 Informationen identifizieren |
in Texten, Tabellen oder grafischen Darstellungen mit chemischen Inhalten die relevanten Informationen identifizieren und sachgerecht interpretieren. |
|
K3 Untersuchungen dokumentieren |
Fragestellungen, Überlegungen, Handlungen und Erkenntnisse bei Untersuchungen strukturiert dokumentieren und stimmig rekonstruieren. |
|
K4 Daten aufzeichnen und darstellen |
zur Darstellung von Daten angemessene Tabellen und Diagramme anlegen und skalieren, auch mit Tabellenkalkulationsprogrammen. |
|
K5 Recherchieren |
selbstständig chemische und technische Informationen aus verschiedenen Quellen beschaffen, einschätzen, zusammenfassen und auswerten. |
|
K6 Informationen umsetzen |
aus Informationen sinnvolle Handlungsschritte ableiten und auf dieser Grundlage zielgerichtet handeln. |
|
K7 Beschreiben, präsentieren, begründen |
Arbeitsergebnisse adressatengerecht und mit angemessenen Medien und Präsentationsformen fachlich korrekt und überzeugend präsentieren. |
|
K8 Zuhören, hinterfragen |
bei Diskussionen über chemische Themen Kernaussagen eigener und fremder Ideen vergleichend darstellen und dabei die Perspektive wechseln. |
|
K9 Kooperieren und im Team arbeiten |
beim naturwissenschaftlichen Arbeiten im Team Verantwortung für Arbeitsprozesse und Produkte übernehmen und Ziele und Aufgaben sachbezogen aushandeln. |
Kompetenzbereich Bewertung
Schülerinnen und Schüler können …
|
B1 Bewertungen an Kriterien orientieren |
für Entscheidungen in chemisch-technischen Zusammenhängen Bewertungskriterien angeben und begründet gewichten. |
|
B2 Argumentieren und Position beziehen |
in Situationen mit mehreren Entscheidungsmöglichkeiten kriteriengeleitet Argumente abwägen, einen Standpunkt beziehen und diesen gegenüber anderen Positionen begründet vertreten. |
|
B3 Werte und Normen berücksichtigen |
Konfliktsituationen erkennen und bei Entscheidungen ethische Maßstäbe sowie Auswirkungen eigenen und fremden Handelns auf Natur, Gesellschaft und Gesundheit berücksichtigen. |
Die folgende Übersicht beschreibt die Inhaltsfelder der zweiten Progressionsstufe sowie die ihnen zugeordneten konkretisierten Kompetenzerwartungen. Die Darstellung folgt dabei den Gesichtspunkten, die bereits für die erste Stufe beschrieben wurden. Kompetenzerwerb ist kumulativ. Es wird deshalb erwartet, dass Schülerinnen und Schüler bereits früher erworbene Kompetenzen sowie die in diesem Kapitel beschriebenen Kompetenzen im weiteren Unterricht vertiefen und auch in anderen Zusammenhängen nutzen.
Inhaltsfeld Elemente und ihre Ordnung (5)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
|
|
Basiskonzept Chemische Reaktion Elementfamilien Basiskonzept Struktur der Materie Protonen, Neutronen, Elektronen, Elemente, Atombau, atomare Masse, Isotope, Kern-Hülle-Modell, Schalenmodell Basiskonzept Energie Energiezustände |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- den Aufbau des Periodensystems in Hauptgruppen und Perioden erläutern. (UF1)
- den Aufbau eines Atoms mit Hilfe eines differenzierten Kern-Hülle-Modells beschreiben. (UF1)
- ausgewählte Elemente anhand ihrer charakteristischen Eigenschaften ihren Elementfamilien (Alkalimetalle, Halogene, Edelgase) zuordnen. (UF3)
- aus dem Periodensystem der Elemente wesentliche Informationen zum Atombau von Elementen der Hauptgruppen entnehmen. (UF3, UF4)
- die charakteristische Reaktionsweise eines Alkalimetalls mit Wasser erläutern und diese für andere Elemente verallgemeinern. (UF3)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- mit Hilfe eines differenzierten Atommodells den Unterschied zwischen Atom und Ion darstellen. (E7)
- besondere Eigenschaften von Elementen der 1., 7. und 8. Hauptgruppe mit Hilfe ihrer Stellung im Periodensystem erklären. (E7)
- zeigen (u. a. an der Entwicklung von Atommodellen) dass theoretische Modelle darauf zielen, Zusammenhänge nicht nur zu beschreiben, sondern auch zu erklären. (E9)
Kommunikation
Die Schülerinnen und Schüler können …
- sich im Periodensystem anhand von Hauptgruppen und Perioden orientieren und hinsichtlich einfacher Fragestellungen zielgerichtet Informationen zum Atombau entnehmen. (K2)
Bewertung
Die Schülerinnen und Schüler können …
- Vorstellungen zu Teilchen, Atomen und Elementen, auch in ihrer historischen Entwicklung, beschreiben und beurteilen und für gegebene Fragestellungen ein angemessenes Modell zur Erklärung auswählen. (B3, E9)
Inhaltsfeld Säuren, Laugen, Salze (6)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
Eigenschaften saurer und alkalischer Lösungen
Salze und Mineralien |
|
|
Basiskonzept Chemische Reaktion Neutralisation, Hydration, pH-Wert, Indikatoren Basiskonzept Struktur der Materie Elektronenpaarbindung, Wassermolekül als Dipol, Wasserstoffbrückenbindung, Protonenakzeptor und –donator, Ionenbindung und Ionengitter Basiskonzept Energie exotherme und endotherme Säure-Base-Reaktionen |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- Beispiele für saure und alkalische Lösungen nennen und ihre Eigenschaften beschreiben. (UF1)
- Säuren bzw. Basen als Stoffe einordnen, deren wässrige Lösungen Wasserstoff-Ionen bzw. Hydroxid-Ionen enthalten. (UF3)
- die Bedeutung einer pH-Skala erklären. (UF1)
- an einfachen Beispielen die Elektronenpaarbindung erläutern. (UF2)
- die räumliche Struktur und den Dipolcharakter von Wassermolekülen mit Hilfe der polaren Elektronenpaarbindung erläutern. (UF1)
- am Beispiel des Wassers die Wasserstoff-Brückenbindung erläutern. (UF1)
- die Salzbildung bei Neutralisationsreaktionen an Beispielen erläutern. (UF1)
- an einem Beispiel die Salzbildung bei einer Reaktion zwischen einem Metall und einem Nichtmetall beschreiben und dabei energetische Veränderungen einbeziehen. (UF1)
- Stoffmengenkonzentrationen an einfachen Beispielen saurer und alkalischer Lösungen erklären. (UF1)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- mit Indikatoren Säuren und Basen nachweisen und den pH-Wert von Lösungen bestimmen. (E3, E5, E6)
- die Bildung von Säuren und Basen an Beispielen wie Salzsäure und Ammoniak mit Hilfe eines Modells zum Protonenaustausch erklären. (E7)
- den Aufbau von Salzen mit Modellen der Ionenbindung und das Lösen von Salzkristallen in Wasser mit dem Modell der Hydration erklären. (E8, UF3)
- Neutralisationen mit vorgegebenen Lösungen durchführen. (E2, E5)
- die Leitfähigkeit einer Salzlösung mit einem einfachen Ionenmodell erklären. (E5)
Kommunikation
Die Schülerinnen und Schüler können …
- unter Verwendung von Reaktionsgleichungen die chemische Reaktion bei Neutralisationen erklären und die entstehenden Salze benennen. (K7, E8)
- in einer strukturierten schriftlichen Darstellung chemische Abläufe sowie Arbeitsprozesse und Ergebnisse (u. a. einer Neutralisation) erläutern. (K1)
- inhaltliche Nachfragen zu Beiträgen von Mitschülerinnen und Mitschülern sachlich und zielgerichtet formulieren. (K8)
- sich mit Hilfe von Gefahrstoffhinweisen und entsprechenden Tabellen über die sichere Handhabung von Lösungen informieren. (K2, K6)
Bewertung
Die Schülerinnen und Schüler können …
- beim Umgang mit Säuren und Laugen Risiken und Nutzen abwägen und entsprechende Sicherheitsmaßnahmen einhalten. (B3)
- die Verwendung von Salzen unter Umwelt- bzw. Gesundheitsaspekten kritisch reflektieren. (B1)
Inhaltsfeld Elektrische Energie aus chemischen Reaktionen (7)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
Batterie und Akkumulator
|
Mobile Energiespeicher |
|
Basiskonzept Chemische Reaktion Umkehrbare und nicht umkehrbare Redoxreaktionen Basiskonzept Struktur der Materie Elektronenübertragung, Donator-Akzeptor-Prinzip Basiskonzept Energie Elektrische Energie, Energieumwandlung, Energiespeicherung |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- Reaktionen zwischen Metallatomen und Metallionen als Redoxreaktionen deuten, bei denen Elektronen übergehen. (UF1)
- den grundlegenden Aufbau und die Funktionsweise von Batterien, Akkumulatoren und Brennstoffzellen beschreiben. (UF1, UF2, UF3)
- elektrochemische Reaktionen, bei denen Energie umgesetzt wird, mit der Aufnahme und Abgabe von Elektronen nach dem Donator-Akzeptor-Prinzip deuten. (UF3)
- die Elektrolyse und die Synthese von Wasser durch Reaktionsgleichungen unter Berücksichtigung energetischer Aspekte darstellen. (UF3)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- einen in Form einer einfachen Reaktionsgleichung dargestellten Redoxprozess in die Teilprozesse Oxidation und Reduktion zerlegen. (E1)
Die Schülerinnen und Schüler können …
- schematische Darstellungen zum Aufbau und zur Funktion elektrochemischer Energiespeicher adressatengerecht erläutern. (K7)
- aus verschiedenen Quellen Informationen zur sachgerechten Verwendung von Batterien und Akkumulatoren beschaffen, ordnen, zusammenfassen und auswerten. (K5)
- Informationen zur umweltgerechten Entsorgung von Batterien und Akkumulatoren umsetzen. (K6)
Bewertung
Die Schülerinnen und Schüler können …
- Kriterien für die Auswahl unterschiedlicher elektrochemischer Energiewandler und Energiespeicher benennen und deren Vorteile und Nachteile gegeneinander abwägen. (B1, B2)
Inhaltsfeld Stoffe als Energieträger (8)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
|
|
|
Basiskonzept Chemische Reaktion alkoholische Gärung Basiskonzept Struktur der Materie Kohlenwasserstoffmoleküle, Strukturformeln, funktionelle Gruppe, Unpolare Elektronenpaarbindung, Van-der-Waals-Kräfte Basiskonzept Energie Katalysator, Treibhauseffekt, Energiebilanzen |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- Beispiele für fossile und regenerative Energierohstoffe nennen und die Entstehung und das Vorkommen von Alkanen in der Natur beschreiben. (UF1)
- die Fraktionierung des Erdöls erläutern. (UF1)
- den grundlegenden Aufbau von Alkanen und Alkanolen als Kohlenwasserstoffmoleküle erläutern und dazu Strukturformeln benutzen. (UF2, UF3)
- typische Stoffeigenschaften von Alkanen und Alkanolen mit Hilfe der Molekülstruktur und zwischenmolekularen Kräften auf der Basis der unpolaren und polaren Elektronenpaarbindung erklären. (UF3, UF2)
- an einfachen Beispielen Isomerie erklären und Nomenklaturregeln anwenden. (UF2, UF3)
- die Eigenschaften der Hydroxylgruppe als funktionelle Gruppe beschreiben. (UF1)
- die Erzeugung und Verwendung von Alkohol und Biodiesel als regenerative Energierohstoffe beschreiben. (UF4)
- die Bedeutung von Katalysatoren beim Einsatz von Benzinmotoren beschreiben. (UF2, UF4)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- für die Verbrennung von Alkanen eine Reaktionsgleichung in Worten und in Formeln aufstellen. (E8)
- bei Alkanen die Abhängigkeit der Siede- und Schmelztemperaturen von der Kettenlänge beschreiben und damit die fraktionierte Destillation von Erdöl erläutern. (E7)
- naturwissenschaftliche Fragestellungen im Zusammenhang mit der Diskussion um die Nutzung unterschiedlicher Energierohstoffe erläutern. (E1)
- bei Verbrennungsvorgängen fossiler Energierohstoffe Energiebilanzen vergleichen. (E6)
- aus natürlichen Rohstoffen durch alkoholische Gärung Alkohol herstellen. (E1, E4, K7)
Kommunikation
Die Schülerinnen und Schüler können …
- die Begriffe hydrophil und lipophil anhand von einfachen Skizzen oder Strukturmodellen und mit einfachen Experimenten anschaulich erläutern. (K7)
- anhand von Sicherheitsdatenblättern mit eigenen Worten den sicheren Umgang mit brennbaren Flüssigkeiten und weiteren Gefahrstoffen beschreiben. (K6)
- die Zuverlässigkeit von Informationsquellen (u. a. zur Entstehung und zu Auswirkungen des natürlichen und anthropogenen Treibhauseffektes) kriteriengeleitet einschätzen. (K5)
Bewertung
Die Schülerinnen und Schüler können …
- Vor- und Nachteile der Nutzung fossiler und regenerativer Energierohstoffe unter ökologischen, ökonomischen und ethischen Aspekten abwägen. (B2, B3)
Inhaltsfeld Produkte der Chemie (9)
|
Inhaltliche Schwerpunkte |
Mögliche Kontexte |
Nanoteilchen und neue Werkstoffe |
Kunststoffe und Klebstoffe
Anwendungen der Chemie in Medizin, Natur und Technik |
|
Basiskonzept Chemische Reaktion Synthese von Makromolekülen aus Monomeren, Esterbildung Basiskonzept Struktur der Materie Funktionelle Gruppen, Tenside, Nanoteilchen |
|
Umgang mit Fachwissen
Die Schülerinnen und Schüler können …
- ausgewählte Aroma- und Duftstoffe als Ester einordnen. (UF1)
- Zusatzstoffe in Lebensmitteln klassifizieren und ihre Funktion und Bedeutung erklären. (UF1, UF3)
- die Verknüpfung zweier Moleküle unter Wasserabspaltung als Kondensationsreaktion und den umgekehrten Vorgang der Esterspaltung als Hydrolyse einordnen. (UF3)
- am Beispiel der Esterbildung die Bedeutung von Katalysatoren für chemische Reaktionen beschreiben. (UF2)
- Beispiele für Nanoteilchen und ihre Anwendung angeben und ihre Größe zu Gegenständen aus dem alltäglichen Erfahrungsbereich in Beziehung setzen. (UF4)
Erkenntnisgewinnung
Die Schülerinnen und Schüler können …
- die Waschwirkung von Tensiden und ihre hydrophilen und hydrophoben Eigenschaften mit Hilfe eines Kugelstabmodells erklären. (E8, E3)
- für die Darstellung unterschiedlicher Aromen systematische Versuche zur Estersynthese planen. (E4)
- Thermoplaste, Duroplaste und Elastomere aufgrund ihres Temperaturverhaltens klassifizieren und dieses mit einer stark vereinfachten Darstellung ihres Aufbaus erklären. (E4, E5, E6, E8)
- an Modellen und mithilfe von Strukturformeln die Bildung von Makromolekülen aus Monomeren erklären. (E7, E8)
Kommunikation
Die Schülerinnen und Schüler können …
- Wege und Quellen beschreiben, um sich differenzierte Informationen zur Herstellung und Anwendung von chemischen Produkten (u. a. Kunststoffe oder Naturstoffe) zu beschaffen. (K5)
- Summen- oder Strukturformeln als Darstellungsform zur Kommunikation angemessen auswählen und einsetzen. (K7)
- eine arbeitsteilige Gruppenarbeit organisieren, durchführen, dokumentieren und reflektieren. (K9)
Bewertung
Die Schülerinnen und Schüler können …
- am Beispiel einzelner chemischer Produkte oder einer Produktgruppe kriteriengeleitet Chancen und Risiken einer Nutzung abwägen, einen Standpunkt dazu beziehen und diesen gegenüber anderen Positionen begründet vertreten. (B2, K8)


 Kontakt
Kontakt